Definice
Elektrochemické zdroje proudu je možné definovat jako zařízení, ve kterých dochází k přímé přeměně chemické energie na energii elektrickou. Látky vstupující do chemické reakce mají jiný obsah vnitřní (utajené) energie nežli reakční produkty. Rozdílem je energie, kterou reagující soustava přijímá nebo dodává svému okolí. Většina samovolně probíhajících chemických reakcí, tedy i vybíjení elektrochemických zdrojů, probíhá tak, že látky vstupující do reakce mají větší obsah vnitřní energie nežli reakční produkty, takže rozdíl energie je dodáván okolí formou tepla, světla, mechanické práce, elektrické energie apod. Elektrochemické zdroje proudu jsou uspořádány tak, aby většina uvolněné energie byla energie elektrická a tak bylo dosaženo co největší účinnosti.
Elektrochemický článek - Základem všech elektrochemických zdrojů proudu je elektrochemický (galvanický) článek, který je tvořen dvojicí elektrod a iontově vodivým elektrolytem, tato soustava je umístěna ve vhodné nádobě. Elektrochemicky aktivní materiál elektrod musí být volen tak, aby na jedné z nich probíhala oxidace a na druhé redukce. Elektroda na které probíhá oxidace se nazývá anoda, elektroda na které probíhá redukce katoda. Elektrody bývají oddělené porézním separátorem, aby se zabránilo přímému kontaktu (zkratu) elektronově vodivých částí elektrod.
Základní rozdělení elektrochemických zdrojů proudu se dělí na primární článek — článek, který není určen k nabíjení elektrickým proudemčlánky primární nebo-li nenabíjecí články, akumulátorový článek — článek, který je určen k nabíjení elektrickým proudemčlánky sekundární nebo-li akumulátory a články palivový článek — článek, který může elektrochemickým procesem přeměňovat chemickou energii z nepřetržitě dodávaných reagujících látek na elektrickou energiipalivové.
Primární články mají pouze schopnost přeměnit při vybíjení chemickou energii na energii elektrickou, ale akumulovat energii již nemají.
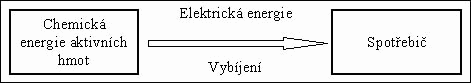
Schématické zobrazení funkce primárního článku
Elektrické akumulátory jsou chemické zdroje elektrické energie, které jsou v průběhu nabíjení schopné přijímat elektrickou energii z vnějšího zdroje a ukládat ji (akumulovat) ve svých elektrodách jako energii chemickou (změnou chemického složení elektrochemicky aktivních složek elektrod). Při vybíjení dodává akumulátor elektrickou energii do spotřebiče, při tom se mění chemické složení aktivních složek elektrod, chemická energie v nich akumulovaná se mění na energii elektrickou. Schématické zobrazení je na obrázku.

Schématické zobrazení funkce akumulátoru
Je důležité si uvědomit, že polarita článku se nezmění, když změníme směr proudu (vybíjení na nabíjení). Při této změně dojde k tomu, že na elektrodě, kde probíhala redukce, bude probíhat oxidace a obráceně. V elektrochemii není termín „katoda“ (elektroda, na níž probíhá redukce) a termín „anoda“ (elektroda, na níž probíhá oxidace) spojen s polaritou článku (plus a minus pól), nýbrž se směrem procházejícího proudu. Tyto termíny mají smysl, jen pokud prochází proud. Proto se používají výrazy kladná elektroda — konstrukční část článku obsahující aktivní materiál, na níž dochází během vybíjení podle konvence k redukční reakcikladná elektroda a záporná elektroda — konstrukční část článku obsahující aktivní materiál, na níž dochází během vybíjení podle konvence k oxydační reakcizáporná elektroda.
Elektrody palivových článků jsou pouze proudový kolektor — sběrač elektrického prouduproudovým kolektorem a místem, kde probíhá elektrochemická reakce; elektrochemicky aktivní látky (plynné, kapalné nebo pevné) jsou do elektrod v průběhu této reakce kontinuálně přiváděny (viz obr. Schématické zobrazení funkce palivového článku), produkty elektrochemické proudotvorné reakce jsou z palivového článku odváděny.
Na dalším obrázku je uveden příklad palivového článku s plynnými elektrochemicky aktivními látkami, kterým je kyslíkovodíkový palivový článek, který jako vstupující materiály využívá plynný kyslík a vodík, reakčním produktem je voda. Na dalším obrázku je schématicky znázorněna funkce metanolového palivového článku, který pro elektrochemickou proudotvornou reakci využívá kapalný metylalkohol a plynný vzdušný kyslík, reakčními produkty jsou oxid uhličitý a voda. Příkladem palivového článku s pevnou elektrodou je zinkovzdušný palivový článek, u kterého se elektroda tvořená deskou kovového zinku může po spotřebování mechanicky vyměnit, zatímco vzdušný kyslík je do článku kontinuálně přiváděn.
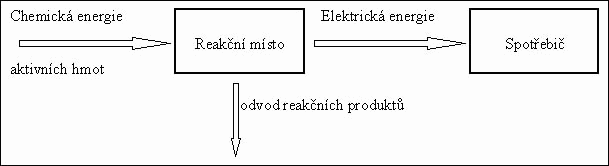
Schématické zobrazení funkce palivového článku
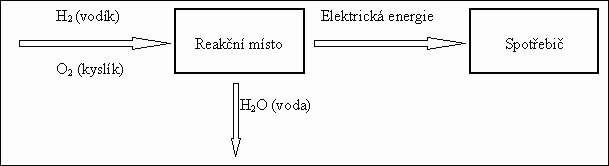
Schématické zobrazení kyslíkovodíkového palivového článku
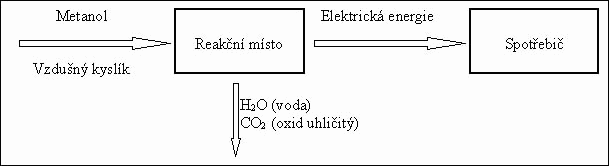
Schématické zobrazení metanolového palivového článku
 Abeceda baterií a akumulátorů
Abeceda baterií a akumulátorů