Princip
Elektrochemicky aktivní složkou kladné elektrody je ve vybitém stavu hydroxid nikelnatý, záporné elektrody hydroxid kademnatý. Elektrochemické děje v průběhu nabíjení a vybíjení je možné velmi zjednodušeně popsat pomocí následující rovnice:
Vedle elektrochemicky aktivní složky obsahují elektrody další materiály, které vytvářejí vodivou složku, nosný skelet a proudový kolektor. elektrolyt — kapalina nebo tuhá látka obsahující pohyblivé ionty, které ji činí iontově vodivou Elektrolytem hermetických akumulátorů je ve většině případů hydroxid draselný (KOH), rozpuštěný ve vodě. Mezi elektrody jsou vloženy separátor (elektrody) — konstrukční část článku vyrobená z materiálu prostupného pro ionty, který uvnitř článku zabraňuje elektrickému kontaktu mezi elektrodami opačné polarity, ale současně umožňuje kontakt elektrod s elektrolytemseparátory, které oddělují kladný a záporný elektrodový systém a současně slouží jako nosič elektrolytu. Při nabíjení se aktivní složka kladné elektrody, hydroxid nikelnatý, mění na nikloxihydroxid (dvojmocný nikl přechází na trojmocný) a hydroxid kademnatý na kovové kadmium. Tyto děje však mohou probíhat pouze do plného nabití elektrod.
Pokud nabíjení pokračuje i po plném nabití elektrod, dochází k přebíjení, při kterém se začne rozkládat elektrolyt – dochází k elektrolýze vody, jejímž důsledkem je vývoj kyslíku na kladné a vodíku na záporné elektrodě. U otevřených akumulátorů jsou takto vznikající plyny odváděny do okolní atmosféry. V hermetických akumulátorech se využívá schopnosti záporné elektrody vázat kyslík uvolňující se na kladné elektrodě při přebíjení. Tento děj se nazývá rekombinace. Kapacita elektrod musí být nastavena tak, aby při dosažení plného nabití kladné elektrody existovala v záporné elektrodě část aktivní hmoty v nenabitém stavu, to znamená, že záporná elektroda musí mít vůči kladné elektrodě větší kapacitu. Chemické děje probíhající při přebíjení hermetických NiCd akumulátorů je možné velmi zjednodušeně popsat celkovou rovnicí:

2.1 Konstrukce hermetického NiCd akumulátoru válcového tvaru
Výsledným dějem je to, že kyslík uvolněný při přebíjení na kladné elektrodě je vázán na elektrodě záporné. Při tom je kovové kadmium vznikající jako produkt nabíjení záporné elektrody oxidováno na Cd(OH)2, čímž je zabráněno jejímu plnému nabití s následujícím přebíjením a nežádoucím vývojem vodíku. Tento pochod se nazývá rekombinace. Z vnějšího pohledu se proces přebíjení hermetických akumulátorů jeví tak, že článku je dodávána elektrická energie, která se přeměňuje v teplo, článek se zahřívá.
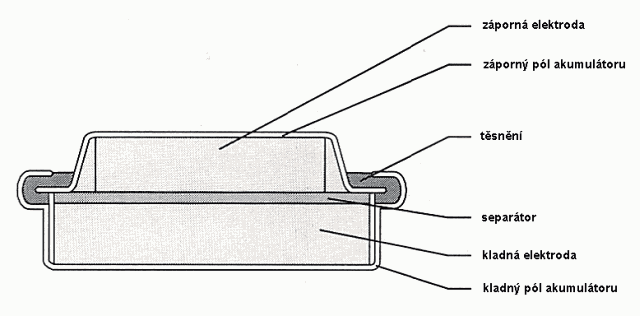
2.2 Konstrukce hermetického NiCd akumulátoru knoflíkového tvaru
 Abeceda baterií a akumulátorů
Abeceda baterií a akumulátorů 2 NiOOH + Cd + 2H2O
2 NiOOH + Cd + 2H2O